Sprawy się skomplikowały dla akcjonariuszy Mabionu (WA:MABP). Wielu z nich liczy na owoce współpracy z Novavaxem, w ramach której polska spółka jest podwykonawcą amerykańskiej firmy biotechnologicznej w zakresie produkcji antygenu niezbędnego dla szczepionek przeciw koronawirusowi. FDA zatroskała się wynikami badań Novavaxu – wskazała, że stosowanie szczepionki może być prowadzić do m.in. zapalenia mięśnia sercowego. W odpowiedzi na te doniesienia kurs Novavaxu zanurkował 20% podczas piątkowej sesji. Nerwowo zareagowała też cena Mabionu. Przez większość piątkowych notowań kurs zachowywał się stabilnie. O zastrzeżeniach FDA jako pierwsza poinformowała agencja Reuters – od pojawienia się depeszy kurs Mabionu solidnie spadł i zakończył dzień ok. 7% przeceną. Scenariusz, gdy AdCom zwołany na 7 czerwca negatywnie głosuje w sprawie szczepionki i/lub taką samą decyzję później podejmuje FDA. Może mieć niekorzystny wpływ na kurs Mabionu – przekonuje Katarzyna Kosiorek, analityczka life sciences Trigon DM.
Przed otwarciem piątkowej sesji giełdowej na rynku amerykańskim pojawiła się w serwisach informacyjnych depesza Reutersa, która zakłopotała akcjonariuszy Novavaxu (ticker: NVAX). Agencja podała, że zdaniem naukowców z FDA szczepionka przeciw koronawirusowi ma skutki uboczne, mimo, że równocześnie doceniono jej skuteczność. Szczepionka Novavaxu działa skutecznie w ponad 90% w zwalczaniu łagodnej, umiarkowanej lub ciężkiej postaci COVID-19 (na bazie populacji ok. 30 tys. dorosłych osób włączonych do badania). U uczestników w wieku od 18 do 64 lat skuteczność była nawet nieznacznie wyższa.
Co do skutków ubocznych – to nic nowego, nie ma cudownego preparatu bez choćby minimalnych skutków ubocznych. Tym razem najwyraźniej te skutki uboczne, w opinii FDA nie okazały się minimalne.
Agencja zauważyła, że odnotowano liczne przypadki zapalenia osierdzia i mięśnia sercowego w czasie, gdy akurat podano pacjentowi szczepionkę. Działo się to zwłaszcza u nastolatków i młodszych mężczyzn w ciągu siedmiu dni po podaniu drugiej dawki.
„Dostępne dane z krótkoterminowej obserwacji sugerują, że u większości osób objawy ustąpiły, choć nie są jeszcze dostępne informacje na temat potencjalnych długoterminowych następstw” – dodali badacze FDA.
Inne dopuszczone do stosowania szczepionki na COVID-19 też były powiązane ze skutkiem ubocznym w postaci zapalenia mięśnia sercowego i osierdzia. Dotyczyło to zwłaszcza tych wytwarzanych przy użyciu technologii mRNA. Tak było na przykład w przypadku szczepionek mRNA konsorcjum Pfizer/BioNTech i Moderny. Szczepionka Novavaxu nie wykorzystuje technologii mRNA. Jest ona oparta na rekombinowanych białkach, podobnie jak szczepionka przeciw grypie. W związku z tym jest łatwiejsza w transporcie i podawaniu. Więcej kluczowych parametrów szczepionki NVAX na tle innych preparatów na poniższej infografice.
Infografika 1 – Parametry charakterystyczne wybranych szczepionych przeciw koronawirusowi
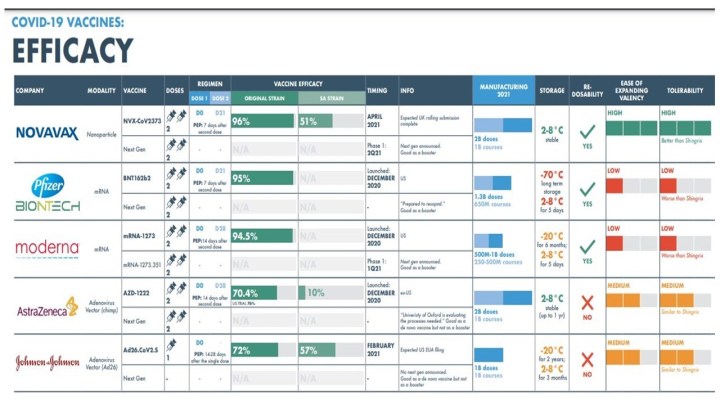
Źródło: RA Capital
Z tą „licznością” przypadków zapalenia, to agencja najwyraźniej trochę przesadziła. Odnotowano raptem pięć przypadków zapalenia mięśnia sercowego i osierdzia. Jeden przypadek mogła spowodować choroba wywołana koronawirusem, a nie szczepionka, jednak nie było jasnych wyjaśnień dla pozostałych przypadków. Cztery przypadki zapalenia serca wystąpiły u młodych mężczyzn, co jest zresztą odzwierciedleniem tego, co zaobserwowano w przypadku szczepionek zawierających mRNA.
Niejasna dla naukowców FDA była też skuteczność szczepionki w odniesieniu do najnowszych mutacji koronawirusa. Trudno się temu dziwić, ponieważ Novavax przeprowadził badanie w okresie od 27 grudnia 2020 roku do 27 września 2021 roku. Było to zatem przed pojawieniem się wariantów Delta i Omicron.
„Odpowiednie dane do oceny skuteczności NVX-CoV2373 przeciwko wariantowi Omicron i podliniom, w tym dane obserwacyjne ze stosowania w innych krajach, w których wdrożono szczepionkę, są obecnie niedostępne” – napisała agencja. „Jednakże, w oparciu o szacunkową skuteczność w badaniu klinicznym tej szczepionki, jest bardziej niż prawdopodobne to, że szczepionka zapewni pewien znaczący poziom ochrony przed COVID-19 z powodu wariantu Omicron, w szczególności przed cięższą chorobą” – dodała.
Dokument, opracowany przez FDA, przeczytasz pod tym linkiem: KLIK.
REPLIKA NOVAVAXU
Novavax, odnosząc się do zastrzeżeń FDA, uspokajał. Z pełną treścią komunikatu zapoznasz się pod tym linkiem: KLIK.
„Dane z badań kontrolowanych przez placebo wykazują, że ogólnie w naszym programie rozwoju klinicznego częstość występowania zapalenia mięśnia sercowego była zrównoważona pomiędzy seriami przyjmowanej szczepionki i placebo (0,007% i 0,005%). Co więcej, w części naszych badań obejmującej okres po przejściu na inny lek, wszystkie zaobserwowane przypadki mieściły się w oczekiwanym zakresie. W oparciu o naszą interpretację wszystkich danych klinicznych wspierających NVX-CoV2373, w tym ponad 50 000 uczestników badań klinicznych, uważamy, że nie ma wystarczających dowodów, aby ustalić związek przyczynowy” – czytamy w komunikacie.
Mimo to akcje NVAX straciły 1/5 wartości podczas piątkowych notowań. Przecenie uległy również akcje Mabionu (ticker: MAB), powiązanego biznesowo z amerykańską korporacją, choć nie była ona tak drastyczna.
Infografika 2 – Zmiana kursu NVAX i MAB w ciągu ostatnich 6 miesięcy
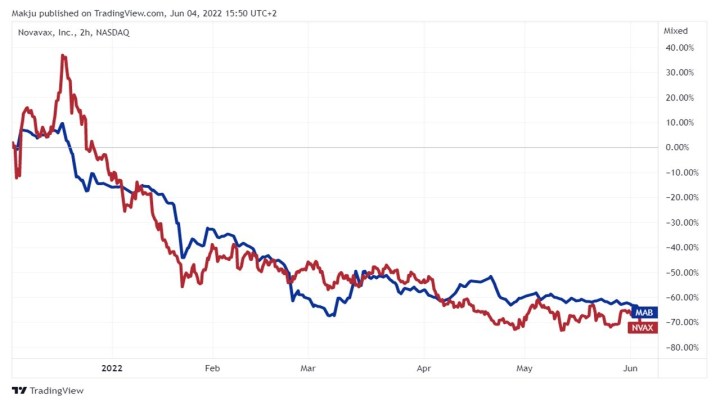
Źródło: Trading View
POROZUMIENIE BIZNESOWE MABIONU Z NOVAVAXEM
W 2021 roku Mabion zawarł z Novavaxem porozumienie (później nieraz rozszerzane) m. in. na produkcję kontraktową antygenu białkowego. Umowa obowiązuje do końca 2025 roku (istnieje w niej możliwość przedłużenia porozumienia). W grudniu 2021 roku MAB „wypuścił” pierwszą serię antygenu. Według szacunków zarządu w latach 2022-2025 spółka dzięki umowie może uzyskać 1,46 mld złotych przychodów ze sprzedaży. Kwota potężna, zważywszy, że na innych polach biznesowych podłódzkiej firmy nie dzieje się zbyt ciekawie. Z treścią prezentacji inwestorskiej MAB na temat warunków współpracy z NVAX zapoznasz się pod tym linkiem: KLIK. (Wyszukaj prezentacji z października 2021 roku).
Dokładnych szczegółów, na jakie rynki miałaby być kierowana produkcja kontraktowa polskiej spółki – brak. Pozostają domysły i spekulacje.
W jednej z ostatnich rekomendacji dla akcji spółki (z maja 2021 roku) Dawid Górzyński, analityk DM PKO BP (WA:PKO) założył, że Mabion będzie głównie odpowiedzialny za produkcję na rynek polski (15 mln dawek rocznie). Reszta (ok. 4 mln sztuk) miałaby znaleźć odbiorców na terenie innych państw europejskich. Gdyby ten tok rozumowania był słuszny, to fakt, czy NVX-CoV2373 zostanie dopuszczony do obrotu w USA w ogóle nie powinien mieć wpływu na zachowanie się kursu MAB lub mieć niewielki wpływ. Oczywiście, o ile w ustaleniach biznesowych z Novavaxem nie ma czegoś, co nie jest znane publicznie. Europejski nadzorca (EMA) dopuścił bowiem do stosowania szczepionkę. To z punktu widzenia generowania wolnych przepływów pieniężnych przez NVAX kwestia wprowadzenia szczepionki do sprzedaży w USA jest istotna. Preparat dopuszczono niemal na całym świecie. Wykluczamy jednak m.in. Stany Zjednoczone, które z racji uwarunkowań populacyjnych są takim brakującym klejnotem w koronie.
Infografika 3 – Kraje, w których szczepionkę Novavaxu dopuszczono do obrotu
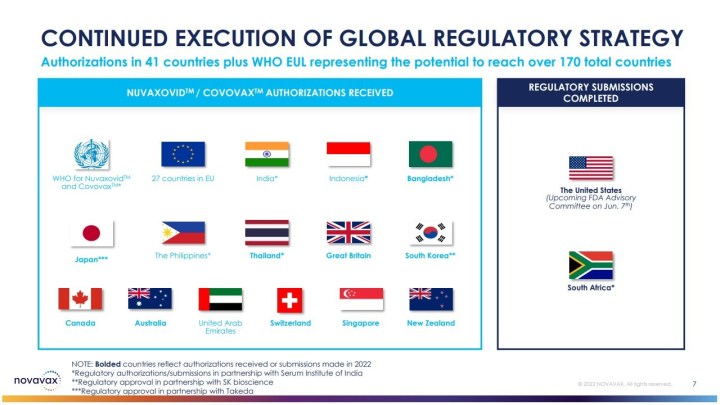
Źródło: Novavax
A zachowanie się kursu akcji MAB jest dość mocno skorelowane ze zmianami ceny NVAX. Widać to choćby po dołączonym wyżej wykresie obu firm za ostatnie 6 miesięcy.
Być może spory wpływ na cenę Mabionu mają oczekiwania co do poziomu kontraktacji podwykonawczej. Zwracała na ten czynnik uwagę pod koniec maja 2022 roku Katarzyna Kosiorek – analityczka Trigon DM. Oceniła ostatnie opublikowane rezultaty kwartalne spółki.
„Pomimo dobrych wyników I kw. 2022, zwracamy uwagę na sytuację pandemiczną i zapotrzebowanie na szczepionki: w kontekście wygaszania pandemii i powszechnej tendencji rozluźniania obostrzeń pandemicznych, począwszy od II pół. 2022 szacujemy ryzyko zmniejszenia kontraktacji zamówień szczepionek na terytorium EU. W kwietniu 2022 polski NFZ poinformował o zawieszeniu dostaw i rozliczeń szczepionek firmy Pfizer. Planowane są zawieszenia dostaw preparatów kolejnych producentów. Identyfikujemy ryzyko zmniejszania kontraktacji zamówień preparatu NVAX na rynku EU, skutkującej mniejszym wolumenem zamówień dla MAB od 2023 roku” – uważa ekspertka. „Z drugiej strony, triggerem wynikowym współpracy NVAX&MAB może być rejestracja preparatu na rynku USA (rynek szczepień antyCOVID-19 w USA w 2022 roku szacowany jest na ok. 21 mld USD wg statista.com)” – dodała.
